Thủ thuật
Nồng độ mol của ion NO3- trong dung dịch Mg(NO3)2 là bao nhiêu?

The concentration of the NO3- ion in a Mg(NO3)2 solution with a molarity of 0.2 M is 0.4 M.
Nồng độ mol của ion NO3 trừ trong dung dịch Mg(NO3)2

Mg(NO3)2 là một muối gồm ion magnesium (Mg2+) và 2 ion nitrat (NO3-). Để tính toán nồng độ mol của ion NO3 trừ trong dung dịch Mg(NO3)2, ta cần biết công thức hóa học và khối lượng mol của các chất.
Trong trường hợp này, từ công thức hóa học của muối Mg(NO3)2, ta có biết rằng để tạo ra một phân tử muối, cần có 1 phân tử magnesium (Mg2+) và 2 phân tử nitrat (NO3-). Vì vậy, nồng độ mol của ion NO3 trừ sẽ bằng gấp đôi nồng độ mol của dung dịch Mg(NO3)2.
Để tính toán nồng độ mol của ion NO3 trừ, ta sử dụng công thức: [NO3-] = 2 * CM(Mg(NO3)2).
Ví dụ, nếu dung dịch Mg(NO3)2 có nồng độ mol là 0.1 M, thì nồng độ mol của ion NO3 trừ sẽ là 0.1 M * 2 = 0.2 M.
Như vậy, để tính toán nồng độ mol của ion NO3 trừ trong dung dịch Mg(NO3)2, ta chỉ cần nhân nồng độ mol của dung dịch Mg(NO3)2 với 2.
Trong dung dịch Mg(NO3)2 0,1 M, nồng độ mol của ion NO3- là 0,2 M.



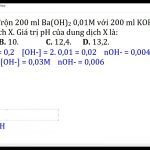
![Tính pH của dung dịch Ba(OH)2 1M: Bước đầu tiên là tính số mol OH- trong 200ml dd Ba(OH)2 1M, sau đó sử dụng công thức pH = 14 + lg[OH-] để tính giá trị pH. Tính pH của dung dịch Ba(OH)2 1M: Bước đầu tiên là tính số mol OH- trong 200ml dd Ba(OH)2 1M, sau đó sử dụng công thức pH = 14 + lg[OH-] để tính giá trị pH.](https://www.panasonic-sky.vn/wp-content/uploads/2023/08/image-88-150x150.jpeg)